Jags, Stan ou Nimble
FinistR 2022
24/08/2022
1 Introduction
Plusieurs outils existent pour réaliser l’inférence bayésienne d’un modèle en générant un échantillon des paramètres sous la loi a posteriori par une chaîne MCMC.
Depuis le premier logiciel Winbugs (codé en Pascal, utilisable seulement sous Windows par presse bouton), plusieurs outils ont été développés, tous appelables depuis R. Les 3 plus utilisés sont les suivants:
WinBUGS : BUGS écrit en Pascal (sur Windows seulement), interface clique-bouton
JAGS : Just Another Gibbs Sampler (Martyn Plummer), package R
rjagsStan : Stanislas Ulaw, co-inventeur des méthodes de Monte Carlo, package R
rstanNimble: Package R écrit par Perry De Valpine.
Nous avons regardé les différences entre JAGS, Stan et Nimble. Les trois peuvent être installés au travers de R.
install.packages("rjags")
install.packages("rstan")
install.packages("nimble")rjags et rstan installent jags
et nimble.
library(rjags)
library(rstan)
library(nimble)JAGS est le plus ancien et implémente un Metropolis Hastings within Gibbs.
Stan implémente un hamiltonian Monte Carlo (marche aléatoire guidée par le gradient de la posterior). La chaîne explore la loi a posteriori de façon plus efficace (donc moins d’itérations nécéssaires) mais chaque itération est plus couteuse. Par ailleurs, stan ne peut être utilisé si certains paramètres (ou même variables latentes) sont discrètes (par de différenciation possible). Voir Saint-Clair pour une discussion plus argumentée.
Nimble permet de choisir son algorithme d’échantillonage de façon plus souple. Il implémente de plus les filtres particulaires.
Tous fonctionnent de la même façon. Il faut d’abord écrire un
modèle dans un fichier txt.
Le modèle est écrit de façon hiérarchique (exactement comme le modèle
d’origine). \[Y | X \sim F(y,X,\theta)
\quad X\sim G(x,\theta) \quad \theta \sim \pi(\theta)\]
Puis ce code est interprété pour générer les chaînes MCMC de loi stationnaire \[p(\theta | Y) \propto \ell(Y | \theta)\pi(\theta).\] Cette souplesse de modèle est à l’origine du succès de l’inférence bayésienne. Cependant, aucun algorithme n’échappe aux problèmes inhérents à l’inférence bayésienne (initialisation, etc…).
2 Exemple jouet de croissance d’orangers
2.1 Les données
On considère les données dans le fichier myOrange.Rdata
qui sont des données (simulées) de croissance d’orangers.
load("myOrange.Rdata")
g <- ggplot(Orange,aes(x=age,y = circumference,colour = Tree)) + geom_point() + geom_line()+theme(legend.position="none")
g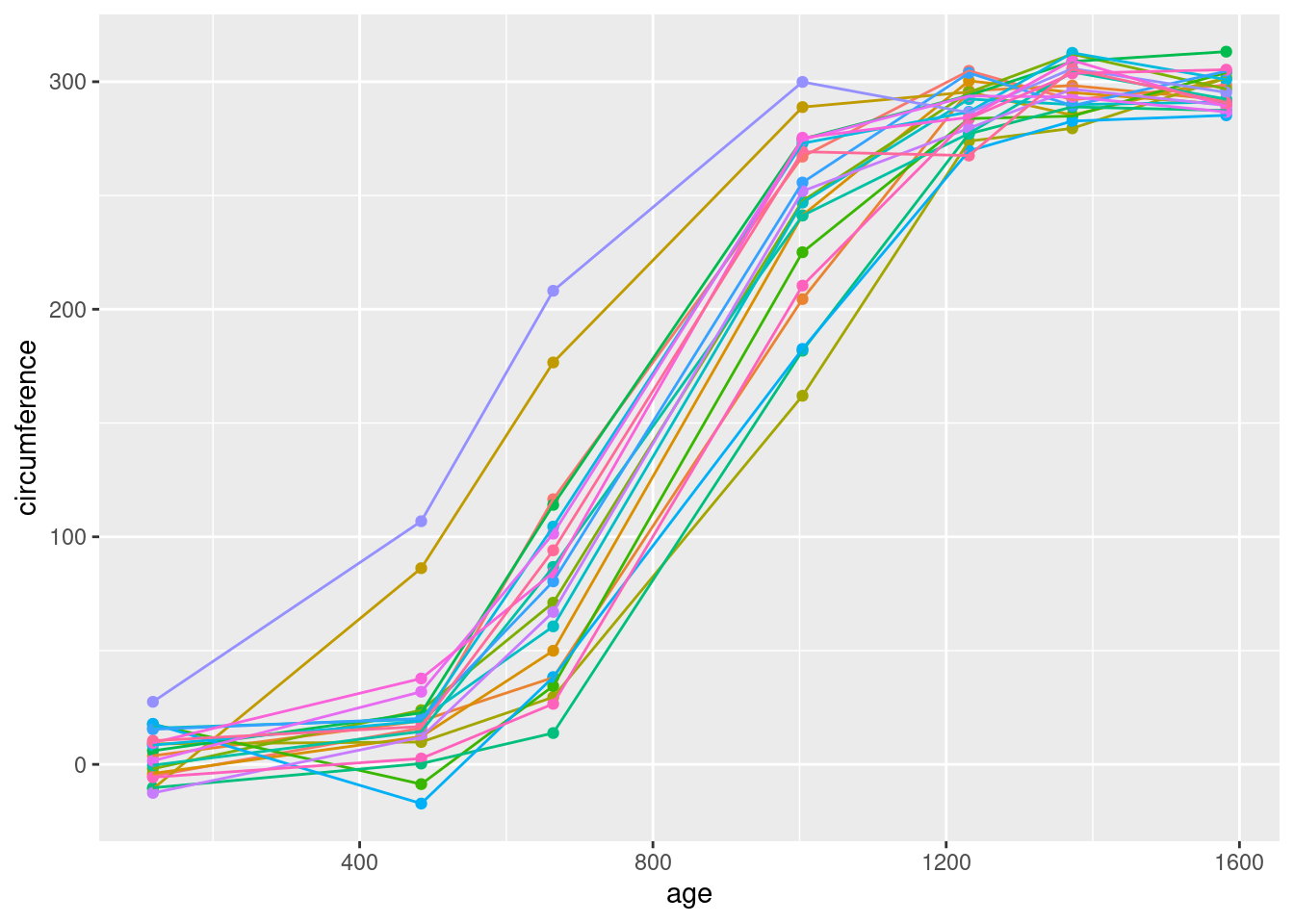
2.2 Le modèle à effets fixes
On considère le modèle de croissance suivant: \[ Y_{ij} = \frac{A}{1+e^{-\left(\frac{ t_{ij} - B}{C}\right)}} + \varepsilon_{ij},\quad \varepsilon_{ij} \sim \mathcal{N}(0,\sigma^2)\]
Les paramètres peuvent être estimés en fréquentiste de la façon suivante:
fm1 <- nls(circumference ~ SSlogis(age, Asym, xmid, scal),data = Orange)
fm1$m$getPars()## Asym xmid scal
## 298.6126 802.2702 133.2991Tous les logiciels demandent de stocker les données dans une liste.
orange_data <- list(
y = Orange$circumference,
age = Orange$age,
n = nrow(Orange)
)Nimble met à part les constantes
orange_data_nimble <- list(
y = Orange$circumference,
age = Orange$age)
orange_constants <- list(n = nrow(Orange))3 Ecriture des modèles dans les différents languages.
Il est possible d’écrire les modèles directement dans un script R ou
bien dans un fichier text qui sera sauvé sous le format
.txt pour JAGS et .stan pour Stan. Il est
aussi possible de définir le modèle comme un objet R (chaîne de
caractère).
C’est là que réside la différence pour l’utilisateur entre les outils. La structure est globalement la même, mais il y a des petites différences dans les noms de fonctions. De plus, Stan demande de déclarer les types d’objets.
3.1 Modèle sous JAGS
model_jags="
model{
# observations
for (i in 1:n){
y[i] ~ dnorm(mu[i],tau)
mu[i] <- (A)/(1+exp(-(age[i]- B)/(C)))
}
# priors
tau ~ dgamma(10,2000)
A ~ dnorm(100,1/100000)
B ~ dnorm(100,1/100000)
C ~ dnorm(100,1/100000)
# quantities of interest
sigma2 <- 1/tau
}
"Le modèle est construit par jags.models.
chains <- 3
growth_inits <- list(tau = rgamma(1,10,2000),
A = rnorm(1,200,30),
B = rnorm(1,700,200),
C = rnorm(1,300,100))
myJAGSmodel <- jags.model(textConnection(model_jags), data = orange_data,inits = growth_inits , n.chains = chains,n.adapt = 1000)## Compiling model graph
## Resolving undeclared variables
## Allocating nodes
## Graph information:
## Observed stochastic nodes: 140
## Unobserved stochastic nodes: 4
## Total graph size: 334
##
## Initializing model3.2 Modèle sous Nimble
C’est la même écriture que sous Jags qu’on commence par une accolade
{.
growth_code_dcat <- nimbleCode({
# observations
for (i in 1:n){
y[i] ~ dnorm(mu[i],tau)
mu[i] <- (A)/(1+exp(-(age[i]- B)/(C)))
}
# priors
tau ~ dgamma(10,2000)
A ~ dnorm(100,1/100000)
B ~ dnorm(100,1/100000)
C ~ dnorm(100,1/100000)
# quantities of interest
sigma2 <- 1/tau
})La fonction nimbleModelpremet de compiler le models.
# Create model
orange_model_nimble <- nimbleModel(code = growth_code_dcat,
constants = orange_constants,
data = orange_data_nimble, # data can be set later
inits = growth_inits # inits can be set later.
)## Defining model## Building model## Setting data and initial values## Running calculate on model
## [Note] Any error reports that follow may simply reflect missing values in model variables.## Checking model sizes and dimensions3.3 Modèle sous Stan
Ecrit dans un fichier .stan A noter que Rstudio offre
des templates de modèles/fichiers stan.
// to be inputted b the user
data {
int<lower=0> n;
vector[n] y;
vector[n] age;
}
// parameters to be sampled
parameters {
real A;
real B;
real C;
real<lower=0> sigma;
}
transformed parameters{
vector[n] mu;
for (i in 1:n)
mu[i] = (A)/(1+exp(-(age[i]- B)/(C)));
}
// model for the likelihood and the priors
model {
for (i in 1:n)
y[i] ~ normal(mu[i], sigma);
A ~ normal(0,100);
B ~ normal(0,100);
C ~ normal(0,100);
}Notez que les 3 outils permettent de compiler et vérifier le modèle. Des fonctions combinants toutes les étapes sont disponibles.
4 Echantillonnage de la posterior
iterations <- 50000
burnin <- 10000
chains <- 34.1 Stan
samples_stan <- stan(file = "modnonlin.stan",data=orange_data, pars = c("sigma", "A","B","C"), include = TRUE, verbose=FALSE,chains = chains,iter=iterations, thin = 10,warmup = burnin)4.2 Jags
update(myJAGSmodel,burnin)
samples_jags <- coda.samples(myJAGSmodel, variable.names = c("sigma2", "A","B","C"), n.iter= iterations ,thin = 10)4.3 Nimble
growth_MCMCconf <- configureMCMC(orange_model_nimble, monitors = c("A",
"B",
"C",
"tau"))
growth_MCMC <- buildMCMC(growth_MCMCconf)
# Compile model
C_growth_model <- compileNimble(orange_model_nimble,showCompilerOutput = TRUE)
C_growth_MCMC <- compileNimble(growth_MCMC, project = orange_model_nimble)
# Run MCMC sampler
samples_nimble <- runMCMC(C_growth_MCMC, niter = 10000,
nburnin = 2000, samplesAsCodaMCMC = TRUE, nchains = chains)5 Analyse des posterior.
A la fin, il est possible de mettre toutes les sorties au même format
et d’analyser la qualité des inférences avec les mêmes packages
(ggmcmc pour les graphes en ggplot et
coda pour le calcul des indicateurs de convergence des
chaînes).
Les packages utiles sont:
library(ggplot2)
library(ggmcmc)
library(coda)Pour tracer des trajectoires et des autocorrelations, on utilise la package ggmcmc. L’outil ggs permet de convertir les sorties des différents outils dans le bon format.
samples.gg <- ggs(samples_stan)
#samples.gg <- ggs(samples_nimble)
#samples.gg <- ggs(samples_jags)
ggs_traceplot(samples.gg) ## ----ploT autocorrelation,
ggs_autocorrelation(samples.gg)Le package ‘coda’ permet de calculer des indicateurs de convergence.
L’échantillon sous ‘stan’ doit être transformé en list.mcmc avec la
fonction As.mcmc.list
## ----ESS,
samples_mcmc_list <- samples_jags
samples_mcmc_list <- samples_nimble
samples_mcmc_list <-As.mcmc.list(samples_stan)
lapply(samples_mcmc_list,effectiveSize)
## ----Gelman----------------------------
gelman.diag(samples_mcmc_list)
## ----Geweke----------------------------------------------------------------------------------------------
geweke.diag(samples_mcmc_list)